Как следует оценивать однородность смешивания премикса?
18 февраля 2022 года Центр оценки лекарственных средств (CDE) опубликовал «Технические рекомендации по исследованию однородности твердых лекарственных форм для перорального применения и однородности центрального блока управления (испытания)», именуемые в дальнейшем «Руководящие принципы». В Руководстве основное внимание уделяется окончательному процессу смешивания, который также основан на общей концепции качества по замыслу. Это связано с тем, что однородность конечной смеси перед операциями сжатия или наполнения является основой обеспечения однородности содержания конечного продукта, а также оптимальной стадией для отбора проб и проведения исследований гомогенности. В принципе, исследование однородности на этом этапе не следует пропускать, а тестирование однородности содержания конечного продукта не следует проводить напрямую. Конечно, любую операцию смешивания в процессе производства можно оценить на предмет однородности, однако требования и стандарты однородности в других процессах в настоящем Руководстве прямо не указаны. Автор делится некоторыми мыслями и обсуждениями, основанными на практическом опыте, полученном в работе.
Обычные процессы производства твердых лекарственных форм для перорального применения включают влажную грануляцию с высоким усилием сдвига, одностадийную грануляцию в псевдоожиженном слое, сухую грануляцию и прямое прессование/наполнение порошком. Процедуры смешивания при производстве твердых лекарственных форм для перорального применения обычно включают по меньшей мере два этапа смешивания: предварительное смешивание и окончательное смешивание, при этом для некоторых продуктов потенциально может потребоваться более двух этапов смешивания. Хотя процесс окончательного смешивания в целом одинаков для разных методов производства, уровни риска на этапе предварительного смешивания различаются из-за разных производственных принципов, что требует дифференцированных подходов к исследованию однородности предварительного смешивания. В соответствии с разделом «Твердые лекарственные формы для перорального применения» издания 2023 года не существует обязательного требования оценивать однородность смешивания во время предварительного смешивания (если применимо). Правильное определение степени исследования однородности смешивания имеет решающее значение для затрат на разработку продукта и контроля качества.
I. Влажная грануляция с высоким сдвигом
При использовании процесса влажной грануляции с высоким усилием сдвига этап предварительного смешивания в идеале должен выполняться внутри влажного гранулятора. Альтернативно, материалы можно сначала смешать в смесителе перед подачей в гранулятор. Если к продукту не предъявляются особые требования, рекомендуется предварительное смешивание в грануляторе, поскольку это сокращает транспортировку материала и использование смесителя, обеспечивая более эффективный рабочий процесс. Для влажной грануляции с высоким усилием сдвига обычно необходимо предварительное смешивание, поскольку оно сводит к минимуму риск получения неравномерных влажных гранул на последующих этапах обработки.
Принципы отбора проб, основанные на руководящих принципах: Точки отбора проб должны быть равномерно распределены и репрезентативны. Учитывая структурные характеристики смесительного оборудования, следует определить мертвые зоны смесительного оборудования, чтобы обеспечить охват всех материалов, представляя при этом места для наихудшего случая. Точки отбора проб предварительного смешивания внутри влажного гранулятора показаны на рисунке ниже.
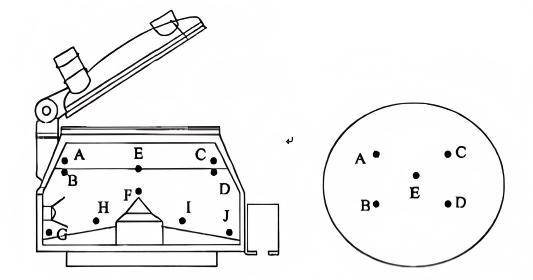
На однородность предварительного смешивания обычно влияют четыре фактора: объем загрузки материала, скорость перемешивания, скорость сдвига и время смешивания, а также потенциальное взаимодействие между ними. Проведение плана экспериментов (DOE) потребует чрезмерного количества испытаний. Объем загрузки можно рассчитать на основе размера окончательной регистрационной партии, чтобы обеспечить согласованность между лабораторными партиями и будущими регистрационными партиями. Скорость перемешивания и скорость сдвига можно определить, учитывая состояние смешивания материалов и соотношение радиусов перемешивающих лопастей между пилотным и промежуточным оборудованием. Этот подход сводит многофакторные переменные к одному параметру — времени смешивания — для анализа.
Начальный этап включает лабораторные исследования для оценки того, как различная продолжительность предварительного смешивания влияет на однородность продукта, что позволяет определить оптимальные параметры. Эти параметры затем проверяются во время пилотного производства. В ходе пилотных операций пробы отбираются с различными интервалами предварительного смешивания для оценки консистенции и обеспечения совместимости времени смешивания в лабораторных и пилотных масштабах. Для проверки процесса требуется только один момент времени, поскольку параметры предварительного смешивания обычно задаются как фиксированные значения, а не диапазоны. Примечательно, что проверка однородности предварительного смешивания на этом этапе часто опускается (особенно для продуктов с низким уровнем риска с маркированными количествами> 25 мг или содержанием активного ингредиента> 25%), поскольку продолжительность смешивания заранее определяется в пилотном производстве, и будет проводиться последующее общее тестирование однородности смешивания.
Основываясь на нашем опыте исследований и разработок лабораторного оборудования, мы разработали предварительные рекомендации по оптимальному времени смешивания. При отборе проб для проверки однородности перед смешиванием пилотной партии нам больше не нужно отбирать три пробы в каждой точке в соответствии со стандартными протоколами. Эта корректировка обусловлена тем, что при оценке пилотной партии основное внимание уделяется оценке того, как различная продолжительность смешивания влияет на однородность. Даже если RSD (относительное стандартное отклонение) в более низкие моменты времени кажется значительным, нет необходимости проверять оставшиеся две выборки на основе результатов измерений. Вместо этого мы должны выбрать оптимальный момент времени, который демонстрирует наибольшую однородность.
Для продуктов гранулирования подпартий, если однородность подпартий перед предварительным смешиванием была изучена в пилотных партиях с хорошей воспроизводимостью между подпартиями, это указывает на стабильные процессы предварительного смешивания. Даже для продуктов с содержанием активного фармацевтического ингредиента (API) ниже 25% риски предварительного смешивания считаются низкими, и проверка однородности предварительного смешивания может быть опущена в партиях для проверки процесса. Персонал, работающий на передовой линии, должен знать, что этап проверки включает в себя исключительно большие объемы выборок и объемы испытаний в сжатые сроки. Благодаря оценке рисков мы можем распределять ресурсы для процессов с высоким риском, чтобы лучше контролировать качество продукции.
II. Одноэтапная грануляция в псевдоожиженном слое
При одностадийной грануляции в псевдоожиженном слое предварительное смешивание обычно не требуется. Материал, подлежащий гранулированию, подается в псевдоожиженный слой, где он подвергается этапу предварительного нагрева (температура регулируется в зависимости от характеристик продукта) для достижения начального смешивания. После этапа предварительного нагрева не требуется никаких испытаний на однородность, что позволяет осуществлять прямую одностадийную грануляцию. В этом процессе используется принцип работы псевдоожиженного слоя, при котором материал остается в состоянии непрерывного кипения, при этом интенсивное перемешивание происходит как на этапе предварительного нагрева, так и на этапе грануляции.
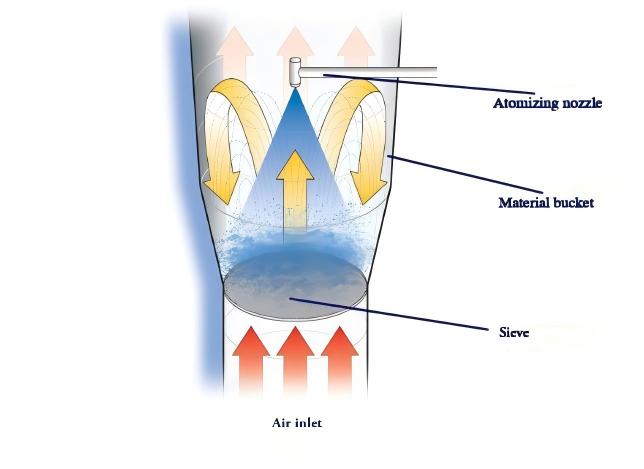
На этапе предварительного нагрева отсутствие добавления связующего может вызвать расслоение материалов разной плотности, что делает оценку однородности после предварительного нагрева нецелесообразной. На последующей фазе грануляции, когда связующее распыляется и вводится, материалы различной плотности связываются друг с другом, постепенно образуя однородные частицы. После грануляции и сушки для повышения выхода продукта необходимы такие операции, как обратная продувка рукавного фильтра. Следовательно, остаточный мелкий порошок или мелкие частицы неизбежно остаются в верхнем слое материала после остановки машины. Таким образом, однородность содержимого, достигаемая за счет одностадийного гранулирования в псевдоожиженном слое, может не соответствовать требованиям, указанным в методических указаниях.
Частицы, полученные посредством одностадийной грануляции в псевдоожиженном слое, могут подвергаться сухой грануляции или поступать непосредственно в процесс маточной смеси, который обеспечивает однородное содержание до прессования/наполнения таблетки. Следовательно, в одностадийных процессах грануляции в псевдоожиженном слое - будь то пилотное испытание, опытно-промышленное производство или проверка процесса - контроль и проверка однородности содержимого могут быть опущены, при этом больший упор делается на стабильность выхода. Если сохраняется проблема единообразия контента, рекомендуется собирать данные для ретроспективного анализа, а не устанавливать строгие критерии приемлемости.
III. Сухая грануляция
В процессах сухой грануляции предварительное смешивание имеет решающее значение для достижения однородного размера частиц, что требует целенаправленных исследований. В отличие от одностадийной грануляции в псевдоожиженном слое, сухая грануляция демонстрирует меньшую эффективность перемешивания. Этап винтового конвейера обеспечивает только локальное смешивание, а условия смешивания материалов, подаваемых в бункер, в конечном итоге определяют однородность сухих гранул.
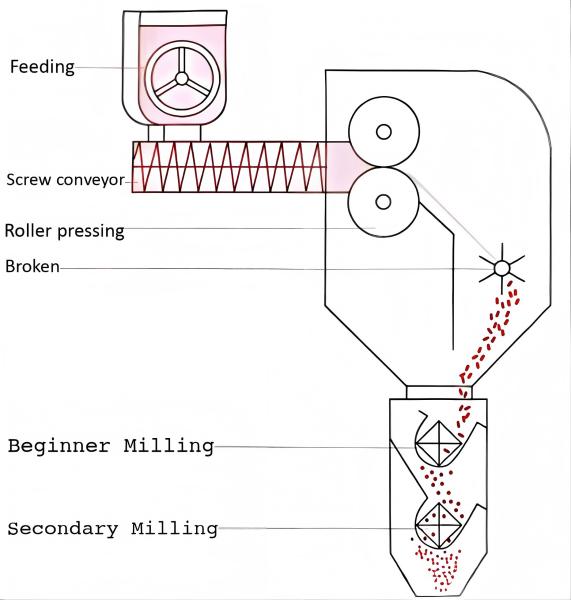
В случае сухого гранулирования после смешивания порошка исследования предварительного смешивания и исследования полного смешивания по существу совпадают. Поскольку один и тот же смеситель можно использовать как для предварительного, так и для полного смешивания, проблемы с подпартиями обычно не возникают во время сухой грануляции после смешивания порошка. Положения отбора проб смесителей разного принципа действия показаны на рисунке ниже.
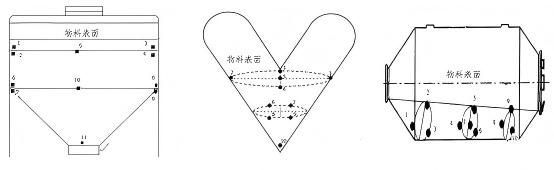
Сухая грануляция в основном применяется для одностадийной грануляции в псевдоожиженном слое, когда определенные типы продуктов имеют низкую плотность (например, твердые дисперсии, приготовленные в псевдоожиженном слое), что требует повышения плотности за счет сухой грануляции для успешного наполнения или прессования таблеток. Возможна обработка субпартий в системах с псевдоожиженным слоем. Поскольку для сухой грануляции обычно требуются внешние добавки, перед обработкой с этими добавками можно объединить несколько партий материалов псевдоожиженного слоя. Оценка однородности предварительной смеси для комбинированных материалов проводится по той же методологии, что и предыдущая процедура смешивания порошков.
Подобно процессу влажной грануляции с высоким усилием сдвига, на основе регистрационной партии можно определить такое же количество загрузки премикса и фиксированную скорость смешивания. От лабораторных пилотных испытаний до пилотных испытаний в цехах можно изучить только влияние времени смешивания. На основании лабораторных пилотных исследований подходящее время предварительного смешивания подтверждается во время пилотной партии. Для продуктов с низким уровнем риска на этапе валидации процесса проводится только одна временная проверка однородности премикса, и проверка однородности предварительного смешивания может быть опущена.
IV. Прямое прессование/наполнение порошками
Процесс прямого прессования/наполнения порошка требует высоких свойств материала для обеспечения качества рецептуры. Обычно существует две стадии смешивания: предварительное смешивание и окончательное смешивание, при этом заключительной стадии предшествует несколько стадий смешивания. В большинстве случаев на заключительном этапе смешивания добавляется лишь небольшое количество смазки или добавки, улучшающей текучесть. Поэтому важно оценить однородность смешивания путем предварительного смешивания и исследований смешивания перед окончательным смешиванием. См. схематическую диаграмму отбора проб в разделе сухого гранулирования.
Исследование однородности в процессе предварительного смешивания/смешивания в первую очередь направлено на определение соответствующих параметров времени смешивания. Учитывая ограниченное количество процессов прямого прессования/наполнения порошком, производство по валидации процесса может одновременно проверять как предварительное смешивание/смешивание, так и окончательное смешивание, чтобы улучшить возможности контроля рисков для производственного процесса.
Процесс прямого прессования/наполнения порошком может включать несколько этапов смешивания, и по возможности следует избегать ручного смешивания на любом из этих этапов. Для продуктов высокого риска воспроизводимость коммерческого производства не может быть гарантирована из-за различий в навыках операторов.
V. Меры предосторожности при смешанных процессах
5.1 Критерии приемки
Для обычных лекарств общая однородность смешивания обычно должна находиться в пределах ±10% (абсолютного) от среднего значения с коэффициентом вариации (RSD) ≤5%. Для препаратов с узким терапевтическим индексом (NTI) или высокоактивных препаратов, где точность разовых доз существенно влияет на эффективность и безопасность препарата, заявителям рецептуры/фармацевтическим производителям рекомендуется на основе научного понимания и оценки риска продукта установить более строгие планы отбора проб, провести исследования однородности смешивания и разработать более строгие критерии приемлемости. Например, если RSD установлено на уровне 2% или даже ниже и предполагается, что коэффициент вариации (CV) <10% для препаратов NTI, однородность содержания 4,5% будет представлять собой значительный риск неэквивалентности биоэквивалентности (БЭ). Обратитесь к разделу анализа эквивалентности в фундаментальной логике препарата BE с узким терапевтическим окном. Независимо от процесса приготовления, достижение того же стандарта однородности предварительного смешивания, что и общая однородность смешивания, является идеальным состоянием. Если однородность предварительного смешивания не может соответствовать соответствующим стандартам, нет необходимости беспокоиться, поскольку приемлемый диапазон однородности предварительного смешивания может быть шире, чем требования, указанные в руководящих принципах, при условии, что общая однородность смешивания соответствует требованиям руководящих принципов.
5.2 время смешивания
На практике полное смешивание обычно включает только добавление стеарата магния в качестве смазывающего вещества в количестве приблизительно 1%. Некоторые специалисты отрасли заметили, что общая продолжительность смешивания устанавливается на уровне 1 или 2 минут, поскольку гомогенность предыдущего этапа смешивания уже проверена до полного смешивания. Даже если стеарат магния распределяется неравномерно во время общего смешивания, такие несоответствия не могут быть обнаружены с помощью теста на однородность общего смешивания. Общая продолжительность смешивания в 1 или 2 минуты может служить просто психологическим успокоением. Неоднородный стеарат магния может привести к различиям в растворении от партии к партии, а также может привести к проблемам с адгезией, что потенциально может привести к необходимости увеличения дозировки стеарата магния.
Как это должно быть спроектировано? Для составов без чрезмерных проблем со смазыванием (когда твердость таблетки ниже ожидаемой или растворение снижено) рекомендуется включать в маточную смесь все внешние материалы, включая стеарат магния, для одновременного смешивания. Этот подход не только исключает один этап обработки, но и позволяет избежать необходимости проведения двух отдельных оценок однородности. Для составов, потенциально склонных к чрезмерному смазыванию, все же можно использовать одноэтапный метод смешивания для достижения кратчайшего времени смешивания для достижения однородности. Стеарат магния затем можно добавлять во время окончательного смешивания маточной смеси в соответствии с этим оптимальным временем. Если кратчайшее время смешивания не может решить проблему чрезмерной смазки (при условии, что смазка действительно избыточная, а не ошибочная оценка, вызванная другими факторами), следует рассмотреть альтернативные смазочные материалы.
5.3 Количество образцов
Согласно рекомендациям, для маточной смеси необходимо отобрать не менее трех проб из каждой точки отбора проб. Для некоторых продуктов может потребоваться дополнительное тестирование на однородность маточной смеси в рамках стандартов качества промежуточной продукции, что требует контроля однородности содержимого во время будущего коммерческого производства. Для премиксов, которые обычно проводятся только на этапе НИОКР и носят исследовательский характер, достаточно от 1 до 2 проб на точку (для резервного копирования).
Объем отбора проб для одного образца обычно должен составлять от 1 до 10 раз больше единичной дозы. Для проверки однородности необходимо использовать всю пробу, чтобы избежать вторичного отбора проб. Если объем пробы превышает в 3 раза единичную дозу, необходимо предоставить научное обоснование или доказательства. Это связано с тем, что объем пробы, превышающий единичную дозу более чем в 3 раза, может маскировать факт неравномерного смешивания из-за чрезмерного количества пробы.
VI. Заключение
В руководящих принципах упоминается, что исследования следует проводить на сортах, которые оцениваются как имеющие средний и высокий риск в процессах смешивания или прессования/наполнения на основе принципа оценки риска в сочетании с характеристиками продукта и производственного процесса. Например, Китайская фармакопея требует изучения однородности смешивания для химических пероральных твердых лекарственных форм (указанное количество <25 мг или содержание активного ингредиента <25%), которые требуют тестирования на однородность содержимого, поскольку риск их смешивания относительно высок. Таким образом, для сортов с низким уровнем риска некоторые исследования процесса предварительного смешивания могут быть сокращены.
Будь то процессы предварительного смешивания или окончательного смешивания, все они должны пройти тщательную оценку и тестирование в соответствии с самыми строгими стандартами. В этом нет никаких сомнений — в конце концов, рецензенты CDE не будут жаловаться на чрезмерные исследования. Однако директора по производству сосредоточат внимание на эффективности и стоимости, особенно во время промежуточных технологических проверок будущего коммерческого производства. Если утверждение контроля качества является обязательным для промежуточных продуктов перед продолжением работы, это не только снижает эффективность производства, но и отклоняется от принципа качества по принципу проектирования. Как разработчики лекарств, мы должны учитывать как этапы исследований и разработок, так и этапы коммерческого производства. Основываясь на характеристиках продукта и оценке рисков, мы должны разработать соответствующие стратегии контроля качества, включая средства контроля для конкретной позиции и суррогатные индикаторы.


















